Accueil / Formation / Manuels / Colposcopie et Traitement des Néoplasies Cervicales Intraépithéliales / Chapitre 12 : Traitement des néoplasies cervicales intraépithéliales par cryothérapie
 figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé...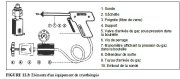 figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 13.3: Instruments nécessair...
figure 13.3: Instruments nécessair... figure 4.9: Spéculum vaginal recou...
figure 4.9: Spéculum vaginal recou...
 figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé... figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 12.4: Unité de cryothérapie...
figure 12.4: Unité de cryothérapie...
 table 12.1: Critères d'éligibilité...
table 12.1: Critères d'éligibilité...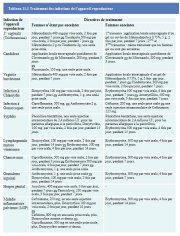 table 11.1: Traitement des infecti...
table 11.1: Traitement des infecti...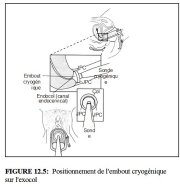 figure 12.5: Positionnement de l'e...
figure 12.5: Positionnement de l'e... figure 12.6: Cryocongélation en co...
figure 12.6: Cryocongélation en co...
 figure 12.5: Positionnement de l'e...
figure 12.5: Positionnement de l'e... figure 12.6: Cryocongélation en co...
figure 12.6: Cryocongélation en co... figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé... figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 12.4: Unité de cryothérapie...
figure 12.4: Unité de cryothérapie...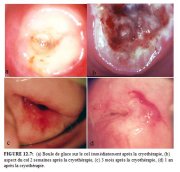 figure 12.7: (a) Boule de glace su...
figure 12.7: (a) Boule de glace su...
 figure 12.7: (a) Boule de glace su...
figure 12.7: (a) Boule de glace su...
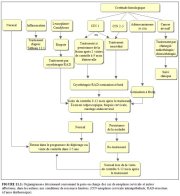 figure 11.1: Flow chart of managem...
figure 11.1: Flow chart of managem...
Colposcopie et Traitement des Néoplasies Cervicales Intraépithéliales : Manuel à l'usage des débutants, édité par J.W. Sellors et R. Sankaranarayanan
Chapitre 12 : Traitement des néoplasies cervicales intraépithéliales par cryothérapie
Autre langue: English / Français / Español / Portugues / ">中文- Dans le cadre du traitement des CIN, la cryothérapie et la résection à lanse diathermique (RAD) représentent des solutions thérapeutiques appropriées et efficaces, autant dans les milieux favorisés que dans les milieux pauvres, car elles requièrent toutes deux un moindre investissement financier en terme déquipement et dentretien, et leur apprentissage est relativement rapide.
- Comparé à léquipement requis pour la RAD, le coût de la cryothérapie est nettement inférieur.
- La cryothérapie dépend dun approvisionnement régulier en gaz réfrigérant liquide contenu dans un réservoir transportable (N2O ou CO2). Cependant, la cryothérapie ne permet pas de traiter les lésions affectant lendocol.
- Quand on parvient à mettre parfaitement en contact la sonde cryogénique avec lexocol, la cryothérapie est réussie lorsque la température au centre de la boule de glace formée par le tissu atteint 89°C pour le système à N2O ou -68°C pour celui à CO2. Sur les bords du tissu congelé, la température est denviron 20°C. Les cellules exposées à 20°C pendant une ou deux minutes entament un processus de cryonécrose.
- La cicatrisation a lieu au cours des six premières semaines suivant la cryothérapie. Les patientes peuvent se plaindre de pertes vaginales liquides pendant 3-4 semaines après le traitement.
- Il faut conseiller aux patientes de ne pas procéder à des douches vaginales, de ne pas utiliser des tampons vaginaux ou de sabstenir davoir des rapports sexuels dans le mois qui suit le traitement.
- La cryothérapie semble susceptible daugmenter la transmissibilité de linfection à VIH et lemploi de préservatifs est un moyen de prévention efficace.
- On constate léchec du traitement dans environ 5-10% des cas.
Les traitements par destruction et par exérèse constituent deux formes de traitement chirurgical de la néoplasie cervicale intraépithéliale (CIN) en consultation externe. Parmi les traitements par destruction des CIN, on distingue la cryothérapie, lélectrocoagulation, la coagulation à froid et la vaporisation au laser. Quant au traitement par exérèse des CIN le plus fréquemment utilisé en consultation externe, il sagit de la résection à lanse diathermique (RAD) qui consiste en une excision cylindrique à laide dune fine électrode métallique en forme d'anse et, éventuellement, dune électrode à aiguille longue.
De tous les traitements efficaces des CIN, la cryothérapie et la RAD sont les seuls à être appropriés à la fois dans les milieux favorisés et dans les milieux aux ressources limitées, ceci pour plusieurs raisons : premièrement, ce sont ceux qui exigent le moins dinvestissement financier pour lachat du matériel, son entretien et sa réparation ; deuxièmement, une fois que la colposcopie est maîtrisée, la cryothérapie et la RAD peuvent être rapidement apprises et donnent de forts taux de guérison avec très peu de complications. Cest pourquoi, nous ne traiterons dans ce manuel que de ces deux techniques. Il existe bien entendu dautres approches chirurgicales faisant appel aux techniques du laser ou de lélectrocoagulation, mais elles sortent du cadre de cet ouvrage. Par ailleurs, il existe sur ce sujet dexcellents livres auxquels létudiant pourra se référer (Wright et al., 1992; Wright et al., 1995; Singer & Monaghan, 2000).
Quand on traite une CIN par destruction ou exérèse, il faut avant tout sinquiéter de savoir si le traitement sera approprié à léradication de toute CIN qui sétendrait jusque dans les cryptes sous-jacentes à lépithélium prénéoplasique. Plus la gravité de la CIN augmente, plus la lésion affecte les cryptes en profondeur. Pour détruire une CIN 3, le traitement doit être efficace jusquà une profondeur de 7 mm. Il faut également considérer un autre facteur : le diametre/surface de la lésion. Cette étendue correspond à la somme de deux distances prises chacune à partir dun point de référence au niveau de lorifice externe : la distance jusquau bord proximal (vers ou dans le canal) et la distance jusquau bord distal de la lésion (loin du canal). Létendue linéaire moyenne est denviron 7.5 mm (entre 2 et 22 mm) avec 85 à 90% des lésions entièrement visibles sur la zone de remaniement à lextérieur du canal (Wright et al., 1995). Lextension dans le vagin ne concerne pas plus de 5% des patientes.
Ce chapitre traite des principes et de la pratique de la cryothérapie. Ceux de la RAD feront lobjet du chapitre suivant. Le coût dachat et dentretien de léquipement nécessaire à la cryothérapie (Figures 12.1, 12.2, et 12.3) est bien inférieur à celui de la RAD, et contrairement à cette dernière, la cryothérapie ne nécessite aucune source délectricité. Elle dépend en effet uniquement dun approvisionnement régulier en gaz réfrigérant liquide contenu dans des réservoirs (bouteilles) facilement transportables.
De plus, contrairement à la RAD, la cryothérapie ne nécessite pas déquipement annexe. En effet, ce type dintervention ne demande aucune anesthésie locale préalable tandis que la RAD requiert plusieurs injections dun anesthésique local dans lexocol. Dautre part, la RAD nécessite aussi un système daspiration afin dévacuer la fumée produite au cours de lintervention et qui stagne dans le vagin masquant ainsi le champ opératoire. Enfin, la RAD exige lemploi dun spéculum vaginal électriquement isolé (et si nécessaire dun rétracteur des parois vaginales également isolé) (Figure 13.3) ou dun spéculum métallique isolé à laide dun préservatif en latex (Figure 4.9), ceci afin déviter tout traumatisme dorigine électrique (choc électrique ou brûlure) à la patiente et à lopérateur, si lélectrode venait à toucher linstrument par accident. En effet, un spéculum vaginal métallique conduit lélectricité et peut provoquer un traumatisme dorigine électrique au niveau du vagin si lélectrode vient accidentellement à son contact. Lorsquils sont électriquement isolés, le spéculum vaginal et le rétracteur des parois vaginales coûtent évidemment plus chers.
Au contraire de la RAD qui représente une méthode dexérèse, la cryothérapie est une méthode de destruction. En terme pratique, cela signifie quil ny aura pas déchantillon de tissu à analyser après une cryothérapie, ce qui constitue évidemment une économie immédiate. Les partisans de la RAD apprécient cependant le retour dinformation qui leur est donné par lanalyse pathologique du tissu excisé. Ce retour dinformation permet non seulement de préciser le grade le plus sévère de la lésion présente, mais également destimer si lexcision est correcte (à savoir si on a bien atteint les bords de la lésion).
La cryothérapie nest pas adaptée au traitement des lésions qui ne sont pas entièrement localisées sur le col et qui plongent dans le canal endocervical. Cest la principale limite de cette technique, tandis que la RAD permet dexciser correctement la majorité des lésions du col même si celles-ci affectent une partie du canal. Une méta-analyse dessais cliniques aléatoires destinés à comparer lefficacité de la cryothérapie avec celle dautres techniques telles que la RAD, la conisation et le laser, a conclu à une efficacité comparable de ces différentes méthodes pour enrayer les CIN (Nuovo et al., 2000; Martin-Hirch et al., 2000). Daprès ces comparaisons et compte tenu de ses avantages, la cryothérapie représente concrètement la méthode la plus pratique et, dun point de vue coût-efficacité, la plus adaptée au traitement des CIN dans les milieux disposant de faibles ressources, à condition bien entendu que la lésion soit entièrement située sur lexocol. Dans le cas contraire, si la lésion affecte le canal endocervical, la RAD sera le traitement de choix (confère Chapitre 13). Une fois le spéculum vaginal en place et le col bien visible, il ne sécoule quune quinzaine de minutes entre le début et la fin de lintervention avec lune ou lautre de ces techniques.
Dans la mesure où la RAD est techniquement plus exigeante que la cryothérapie, nous suggérons aux colposcopistes de prouver dabord leur compétence en matière de cryothérapie avant de passer à la pratique de la RAD.
Lexposition dun tissu vivant à une température de -20°C ou plus basse encore, pendant au moins 1 minute, déclenche une cryonécrose. Ce processus comporte plusieurs aspects : cristallisation intra- et extra-cellulaire, déshydratation, choc thermique, stase vasculaire et dénaturation des protéines. Une rapide congélation suivie dune lente décongélation constitue le traitement le plus destructeur pour des cellules, en particulier des cellules prénéoplasiques. Une série de deux cycles de congélation-décongélation (congélation-décongélation-congélation-décongélation) assure une destruction encore plus efficace.
La cryothérapie est réalisée à laide dune sonde cryogénique dont lextrémité, constituée dun métal très conducteur (généralement en argent ou en cuivre), entre en contact direct avec la surface de la lésion exocervicale. On obtient une importante chute de la température en permettant au gaz liquide réfrigérant de se dilater à travers une petite ouverture de la sonde. Loxyde dazote (N2O) ou le gaz carbonique (CO2) sont les gaz réfrigérants les plus couramment employés car tous deux assurent un excellent transfert thermique lorsquils circulent dans lembout de la sonde.
De tous les traitements efficaces des CIN, la cryothérapie et la RAD sont les seuls à être appropriés à la fois dans les milieux favorisés et dans les milieux aux ressources limitées, ceci pour plusieurs raisons : premièrement, ce sont ceux qui exigent le moins dinvestissement financier pour lachat du matériel, son entretien et sa réparation ; deuxièmement, une fois que la colposcopie est maîtrisée, la cryothérapie et la RAD peuvent être rapidement apprises et donnent de forts taux de guérison avec très peu de complications. Cest pourquoi, nous ne traiterons dans ce manuel que de ces deux techniques. Il existe bien entendu dautres approches chirurgicales faisant appel aux techniques du laser ou de lélectrocoagulation, mais elles sortent du cadre de cet ouvrage. Par ailleurs, il existe sur ce sujet dexcellents livres auxquels létudiant pourra se référer (Wright et al., 1992; Wright et al., 1995; Singer & Monaghan, 2000).
Quand on traite une CIN par destruction ou exérèse, il faut avant tout sinquiéter de savoir si le traitement sera approprié à léradication de toute CIN qui sétendrait jusque dans les cryptes sous-jacentes à lépithélium prénéoplasique. Plus la gravité de la CIN augmente, plus la lésion affecte les cryptes en profondeur. Pour détruire une CIN 3, le traitement doit être efficace jusquà une profondeur de 7 mm. Il faut également considérer un autre facteur : le diametre/surface de la lésion. Cette étendue correspond à la somme de deux distances prises chacune à partir dun point de référence au niveau de lorifice externe : la distance jusquau bord proximal (vers ou dans le canal) et la distance jusquau bord distal de la lésion (loin du canal). Létendue linéaire moyenne est denviron 7.5 mm (entre 2 et 22 mm) avec 85 à 90% des lésions entièrement visibles sur la zone de remaniement à lextérieur du canal (Wright et al., 1995). Lextension dans le vagin ne concerne pas plus de 5% des patientes.
Ce chapitre traite des principes et de la pratique de la cryothérapie. Ceux de la RAD feront lobjet du chapitre suivant. Le coût dachat et dentretien de léquipement nécessaire à la cryothérapie (Figures 12.1, 12.2, et 12.3) est bien inférieur à celui de la RAD, et contrairement à cette dernière, la cryothérapie ne nécessite aucune source délectricité. Elle dépend en effet uniquement dun approvisionnement régulier en gaz réfrigérant liquide contenu dans des réservoirs (bouteilles) facilement transportables.
De plus, contrairement à la RAD, la cryothérapie ne nécessite pas déquipement annexe. En effet, ce type dintervention ne demande aucune anesthésie locale préalable tandis que la RAD requiert plusieurs injections dun anesthésique local dans lexocol. Dautre part, la RAD nécessite aussi un système daspiration afin dévacuer la fumée produite au cours de lintervention et qui stagne dans le vagin masquant ainsi le champ opératoire. Enfin, la RAD exige lemploi dun spéculum vaginal électriquement isolé (et si nécessaire dun rétracteur des parois vaginales également isolé) (Figure 13.3) ou dun spéculum métallique isolé à laide dun préservatif en latex (Figure 4.9), ceci afin déviter tout traumatisme dorigine électrique (choc électrique ou brûlure) à la patiente et à lopérateur, si lélectrode venait à toucher linstrument par accident. En effet, un spéculum vaginal métallique conduit lélectricité et peut provoquer un traumatisme dorigine électrique au niveau du vagin si lélectrode vient accidentellement à son contact. Lorsquils sont électriquement isolés, le spéculum vaginal et le rétracteur des parois vaginales coûtent évidemment plus chers.
Au contraire de la RAD qui représente une méthode dexérèse, la cryothérapie est une méthode de destruction. En terme pratique, cela signifie quil ny aura pas déchantillon de tissu à analyser après une cryothérapie, ce qui constitue évidemment une économie immédiate. Les partisans de la RAD apprécient cependant le retour dinformation qui leur est donné par lanalyse pathologique du tissu excisé. Ce retour dinformation permet non seulement de préciser le grade le plus sévère de la lésion présente, mais également destimer si lexcision est correcte (à savoir si on a bien atteint les bords de la lésion).
La cryothérapie nest pas adaptée au traitement des lésions qui ne sont pas entièrement localisées sur le col et qui plongent dans le canal endocervical. Cest la principale limite de cette technique, tandis que la RAD permet dexciser correctement la majorité des lésions du col même si celles-ci affectent une partie du canal. Une méta-analyse dessais cliniques aléatoires destinés à comparer lefficacité de la cryothérapie avec celle dautres techniques telles que la RAD, la conisation et le laser, a conclu à une efficacité comparable de ces différentes méthodes pour enrayer les CIN (Nuovo et al., 2000; Martin-Hirch et al., 2000). Daprès ces comparaisons et compte tenu de ses avantages, la cryothérapie représente concrètement la méthode la plus pratique et, dun point de vue coût-efficacité, la plus adaptée au traitement des CIN dans les milieux disposant de faibles ressources, à condition bien entendu que la lésion soit entièrement située sur lexocol. Dans le cas contraire, si la lésion affecte le canal endocervical, la RAD sera le traitement de choix (confère Chapitre 13). Une fois le spéculum vaginal en place et le col bien visible, il ne sécoule quune quinzaine de minutes entre le début et la fin de lintervention avec lune ou lautre de ces techniques.
Dans la mesure où la RAD est techniquement plus exigeante que la cryothérapie, nous suggérons aux colposcopistes de prouver dabord leur compétence en matière de cryothérapie avant de passer à la pratique de la RAD.
Lexposition dun tissu vivant à une température de -20°C ou plus basse encore, pendant au moins 1 minute, déclenche une cryonécrose. Ce processus comporte plusieurs aspects : cristallisation intra- et extra-cellulaire, déshydratation, choc thermique, stase vasculaire et dénaturation des protéines. Une rapide congélation suivie dune lente décongélation constitue le traitement le plus destructeur pour des cellules, en particulier des cellules prénéoplasiques. Une série de deux cycles de congélation-décongélation (congélation-décongélation-congélation-décongélation) assure une destruction encore plus efficace.
La cryothérapie est réalisée à laide dune sonde cryogénique dont lextrémité, constituée dun métal très conducteur (généralement en argent ou en cuivre), entre en contact direct avec la surface de la lésion exocervicale. On obtient une importante chute de la température en permettant au gaz liquide réfrigérant de se dilater à travers une petite ouverture de la sonde. Loxyde dazote (N2O) ou le gaz carbonique (CO2) sont les gaz réfrigérants les plus couramment employés car tous deux assurent un excellent transfert thermique lorsquils circulent dans lembout de la sonde.
 figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé... figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 13.3: Instruments nécessair...
figure 13.3: Instruments nécessair... figure 4.9: Spéculum vaginal recou...
figure 4.9: Spéculum vaginal recou...Equipement de cryothérapie (Figures 12.1, 12.2, 12.3 and 12.4)
Une unité de cryothérapie est constituée dune bouteille de gaz liquéfié (réservoir), dun support pourvu dune vis de serrage, dune valve darrivée du gaz permettant de connecter la bouteille de gaz au pistolet cryogénique par lintermédiaire dun tuyau flexible, dun manomètre affichant la pression du gaz, dun détendeur de sortie, dun pistolet cryogénique muni dune poignée et dune gâchette permettant la libération du gaz sous forte pression dans la sonde cryogénique, et enfin, la sonde elle-même. Dans la plupart des équipements, le manomètre affiche trois zones de couleur différente : jaune, verte et rouge. Quand la bouteille de gaz est ouverte, si laiguille indicatrice de la pression passe dans la zone verte, alors cela signifie quil y a assez de pression pour procéder au traitement. En revanche, si laiguille reste dans le jaune, cela signifie quil ny a pas assez de pression ; il faut donc changer la bouteille de gaz avant de commencer lintervention. Enfin, si laiguille bascule dans la zone rouge, il y a trop de pression ; il faut donc en relâcher. Il est vivement conseillé de lire attentivement le manuel opératoire fourni par le constructeur.
 figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé... figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 12.4: Unité de cryothérapie...
figure 12.4: Unité de cryothérapie...Cryothérapie des lésions de lexocol
Le Tableau 12.1 présente les conditions à remplir pour la cryothérapie. Si la patiente souffre dune cervicite, dune trichomoniase ou dune vaginite bactérienne, on lui donnera le choix entre a) une cryothérapie immédiate accompagnée simultanément dun traitement antimicrobien, ou b) un traitement antimicrobien seul, suivi dune cryothérapie deux à trois semaines plus tard (confère Chapitre 11, Tableau 11.1). Si on constate une maladie inflammatoire pelvienne (MIP), il est conseillé dattendre que linfection ait été traitée et guérie avant de procéder à la cryothérapie. Quand on observe une nette atrophie due au manque dstrogènes chez les femmes plus âgées et que la coloration du contour externe de la lésion est indistinct, il est préférable de retarder la cryothérapie jusquà ce quun traitement oestrogénique ait fait son effet et quun diagnostic colposcopique ait été réétabli. Avant de subir une cryothérapie, la patiente doit bien entendu donner son consentement par écrit, non sans avoir été au préalable parfaitement informée du déroulement de lintervention et de ses chances de réussite, des effets secondaires, des complications, des séquelles à long terme, et de toute autre solution de traitement.
Il est conseillé dutiliser la plus grosse bouteille de gaz possible de façon à ne pas tomber en panne de gaz réfrigérant avant la fin du traitement, et à conserver une pression gazeuse suffisamment élevée en bout de sonde tout au long de lintervention pour en garantir lefficacité. Les bouteilles de taille standard permettent de traiter seulement trois patientes à une pression correcte. Si le choix dune bouteille plus grosse présente lavantage de permettre le traitement de plusieurs femmes, en revanche, son transport dun service à lautre peut poser problème.
Quand lembout de la sonde se trouve parfaitement au contact de lexocol (Figures 12.5 et 12.6b), une cryothérapie à lazote permettra datteindre une température denviron -89°C au cur de la boule de glace formée par le tissu, contre -68oC pour une cryothérapie au gaz carbonique. La température sur les bords du tissu congelé est denviron -20oC. Les cellules maintenues à -20oC pendant une minute, ou plus, entameront un processus de cryonécrose. Pour garantir une congélation efficace, la température minimale au niveau de la pointe de la sonde doit être de 60oC. Il est également primordial détablir et de maintenir un excellent contact entre lembout de la sonde et le tissu tout au long de lintervention un contact insuffisant se traduit par de fortes variations de la température atteinte au cur de la boule de glace, et donc par une baisse de lefficacité du traitement sur le tissu cible.
Il est conseillé dutiliser la plus grosse bouteille de gaz possible de façon à ne pas tomber en panne de gaz réfrigérant avant la fin du traitement, et à conserver une pression gazeuse suffisamment élevée en bout de sonde tout au long de lintervention pour en garantir lefficacité. Les bouteilles de taille standard permettent de traiter seulement trois patientes à une pression correcte. Si le choix dune bouteille plus grosse présente lavantage de permettre le traitement de plusieurs femmes, en revanche, son transport dun service à lautre peut poser problème.
Quand lembout de la sonde se trouve parfaitement au contact de lexocol (Figures 12.5 et 12.6b), une cryothérapie à lazote permettra datteindre une température denviron -89°C au cur de la boule de glace formée par le tissu, contre -68oC pour une cryothérapie au gaz carbonique. La température sur les bords du tissu congelé est denviron -20oC. Les cellules maintenues à -20oC pendant une minute, ou plus, entameront un processus de cryonécrose. Pour garantir une congélation efficace, la température minimale au niveau de la pointe de la sonde doit être de 60oC. Il est également primordial détablir et de maintenir un excellent contact entre lembout de la sonde et le tissu tout au long de lintervention un contact insuffisant se traduit par de fortes variations de la température atteinte au cur de la boule de glace, et donc par une baisse de lefficacité du traitement sur le tissu cible.
 table 12.1: Critères d'éligibilité...
table 12.1: Critères d'éligibilité... table 11.1: Traitement des infecti...
table 11.1: Traitement des infecti... figure 12.5: Positionnement de l'e...
figure 12.5: Positionnement de l'e... figure 12.6: Cryocongélation en co...
figure 12.6: Cryocongélation en co...Approche de la cryothérapie étape par étape (Figures 12.5 et 12.6)
La patiente doit remplir les conditions requises pour la cryothérapie rassemblées dans le Tableau 12.1. Il est généralement préférable davoir un diagnostic ferme de CIN avant de procéder à la cryothérapie. Il existe cependant quelques exceptions à cette règle. Ainsi, dans les pays en développement, on proposera parfois cette intervention aux femmes dès leur premier examen colposcopique devant une suspicion de CIN, de façon à maximiser la couverture du traitement établi en fonction du diagnostic colposcopique (si le traitement nest pas appliqué immédiatement, les patientes qui ne se font pas suivre nen recevront aucun). Le prélèvement dune biopsie dirigée avant la cryothérapie permettra dobtenir a posteriori un diagnostic histologique de la nature de la lésion traitée. Les conséquences dune telle approche en termes de traitement excessif ou inutile, ainsi que les effets secondaires et les complications liées à ce type dintervention, doivent être expliqués à la patiente avant de lui demander son consentement éclairé.
Lopérateur doit bien entendu être familier des différents éléments de léquipement de cryothérapie (Figures 12.1-12.4) quil sera amené à utiliser dans un milieu donné. Il est indispensable de lire attentivement la notice fournie par le fabricant concernant la mise en service de lappareil et les règles de sécurité. Ces dernières doivent être suivies à la lettre. Avant de débuter la cryothérapie, il faut vérifier la pression de la bouteille de gaz afin de sassurer quelle est suffisante pour maintenir un débit efficace de gaz réfrigérant à travers lembout de la sonde durant toute la durée de lintervention. A cet égard, on suivra les instructions du fabricant. Dans la plupart des équipements de cryothérapie, si la pression du gaz dans la bouteille est correcte, laiguille du manomètre passera dans le vert (40-70 kg/cm2, dès que la bouteille sera ouverte pour laisser séchapper le gaz. En revanche, si la pression est trop basse, laiguille restera dans la zone jaune (moins de 40 kg/cm2). La pression minimum de travail est de 40 kg par cm2 ; en dessous de cette valeur, la congélation ne sera pas suffisante pour produire la cryonécrose sur toute létendue requise. Dans ce cas, il faudra impérativement changer la bouteille de gaz avant de poursuivre le traitement.
Si la cryothérapie nest pas pratiquée aussitôt après la colposcopie, mais lors dune seconde consultation (après confirmation histologique de la lésion à traiter), il faut renouveler lexamen colposcopique immédiatement avant le traitement afin de sassurer que la localisation et le diamètre/surface de la lésion sont bien compatibles avec une cryothérapie efficace.
Le médecin ou linfirmière doivent expliquer à la patiente le déroulement de lintervention et la rassurer. Il est important de tout mettre en uvre pour laider à rester détendue pendant toute la durée du traitement. Après sêtre assuré quelle a vidé sa vessie, on installe la patiente en position gynécologique, et le col est exposé à laide du spéculum le plus grand possible qui puisse être introduit dans le vagin sans provoquer de gêne. Après avoir débarrassé le col de ses sécrétions à laide dun tampon de coton imbibé de sérum physiologique, on le badigeonne avec une solution dacide acétique à 5% et on lobserve sous le colposcope. Puis, on applique le soluté de Lugol afin de délimiter les contours de la lésion. La cryothérapie ne nécessite aucune anesthésie locale.
La surface de la sonde cryogénique est essuyée avec du sérum physiologique pour garantir le contact thermique avec le col et une chute optimale de la température du tissu. On applique ensuite fermement lembout de la sonde, en plaçant son centre sur lorifice. Il faut impérativement sassurer que la sonde couvre correctement la lésion et que lembout nentre pas en contact par inadvertance avec une partie du vagin quil pourrait geler pendant lintervention. Une fois la minuterie réglée, on presse ou on relâche la gâchette du pistolet cryogénique qui permet le refroidissement de la sonde en contact avec le col. Le gaz séchappe à travers le manomètre avec un sifflement. On peut voir se former de la glace sur lembout de la sonde et sur le col au fur et à mesure que la congélation avance.
La cryothérapie consiste en deux cycles successifs de congélation-décongélation, chacun deux comportant une congélation de 3 minutes suivie dune décongélation de 5 minutes (congélation : 3 minutes - décongélation : 5 minutes congélation : 3 minutes - décongélation). La durée du traitement est chronométrée. La congélation est satisfaisante lorsque la boule de glace dépasse de 4 à 5 mm des bords externes de lembout de la sonde. Cela garantit une cryonécrose sur une profondeur dau moins 5 mm. Pour obtenir un tel effet uniformément sur tout le champ à traiter, il est extrêmement important détablir et de maintenir un contact parfait entre lembout de la sonde et la surface de lexocol. Une fois que la seconde congélation de 3 minutes est achevée, attendez le temps suffisant pour la décongélation avant de retirer la sonde du col. La décongélation est terminée quand il ny a plus de glace sur lembout de la sonde, et celle-ci peut être alors retirée par un délicat mouvement de rotation sur le col. Nessayez surtout pas de retirer la sonde du col avant complète décongélation. Une fois la sonde retirée, vérifiez si le col saigne. La Figure 12.7a montre laspect dun col immédiatement après la cryothérapie. Remarquez la boule de glace qui sest formée dans le col. Après lintervention, il ne faut surtout pas remplir le vagin de gaze ou de coton pour permettre aux sécrétions de sécouler librement. On proposera une serviette hygiénique à la patiente pour éviter que les sécrétions ne tâchent ses vêtements.
Après lemploi, lembout de la sonde doit être essuyée avec de lalcool éthylique ou isopropylique à 60-90%, puis soigneusement nettoyé avec de leau bouillante avant dêtre désinfecté avec du glutaraldehyde à 2% (confère Chapitre 14) et conservé au sec. Une fois lintervention terminée, le pistolet cryogénique, le système de tubes, le manomètre et la bouteille de gaz doivent être décontaminés à laide dun coton imbibé dalcool éthylique ou isopropylique à 60-90%.
Lopérateur doit bien entendu être familier des différents éléments de léquipement de cryothérapie (Figures 12.1-12.4) quil sera amené à utiliser dans un milieu donné. Il est indispensable de lire attentivement la notice fournie par le fabricant concernant la mise en service de lappareil et les règles de sécurité. Ces dernières doivent être suivies à la lettre. Avant de débuter la cryothérapie, il faut vérifier la pression de la bouteille de gaz afin de sassurer quelle est suffisante pour maintenir un débit efficace de gaz réfrigérant à travers lembout de la sonde durant toute la durée de lintervention. A cet égard, on suivra les instructions du fabricant. Dans la plupart des équipements de cryothérapie, si la pression du gaz dans la bouteille est correcte, laiguille du manomètre passera dans le vert (40-70 kg/cm2, dès que la bouteille sera ouverte pour laisser séchapper le gaz. En revanche, si la pression est trop basse, laiguille restera dans la zone jaune (moins de 40 kg/cm2). La pression minimum de travail est de 40 kg par cm2 ; en dessous de cette valeur, la congélation ne sera pas suffisante pour produire la cryonécrose sur toute létendue requise. Dans ce cas, il faudra impérativement changer la bouteille de gaz avant de poursuivre le traitement.
Si la cryothérapie nest pas pratiquée aussitôt après la colposcopie, mais lors dune seconde consultation (après confirmation histologique de la lésion à traiter), il faut renouveler lexamen colposcopique immédiatement avant le traitement afin de sassurer que la localisation et le diamètre/surface de la lésion sont bien compatibles avec une cryothérapie efficace.
Le médecin ou linfirmière doivent expliquer à la patiente le déroulement de lintervention et la rassurer. Il est important de tout mettre en uvre pour laider à rester détendue pendant toute la durée du traitement. Après sêtre assuré quelle a vidé sa vessie, on installe la patiente en position gynécologique, et le col est exposé à laide du spéculum le plus grand possible qui puisse être introduit dans le vagin sans provoquer de gêne. Après avoir débarrassé le col de ses sécrétions à laide dun tampon de coton imbibé de sérum physiologique, on le badigeonne avec une solution dacide acétique à 5% et on lobserve sous le colposcope. Puis, on applique le soluté de Lugol afin de délimiter les contours de la lésion. La cryothérapie ne nécessite aucune anesthésie locale.
La surface de la sonde cryogénique est essuyée avec du sérum physiologique pour garantir le contact thermique avec le col et une chute optimale de la température du tissu. On applique ensuite fermement lembout de la sonde, en plaçant son centre sur lorifice. Il faut impérativement sassurer que la sonde couvre correctement la lésion et que lembout nentre pas en contact par inadvertance avec une partie du vagin quil pourrait geler pendant lintervention. Une fois la minuterie réglée, on presse ou on relâche la gâchette du pistolet cryogénique qui permet le refroidissement de la sonde en contact avec le col. Le gaz séchappe à travers le manomètre avec un sifflement. On peut voir se former de la glace sur lembout de la sonde et sur le col au fur et à mesure que la congélation avance.
La cryothérapie consiste en deux cycles successifs de congélation-décongélation, chacun deux comportant une congélation de 3 minutes suivie dune décongélation de 5 minutes (congélation : 3 minutes - décongélation : 5 minutes congélation : 3 minutes - décongélation). La durée du traitement est chronométrée. La congélation est satisfaisante lorsque la boule de glace dépasse de 4 à 5 mm des bords externes de lembout de la sonde. Cela garantit une cryonécrose sur une profondeur dau moins 5 mm. Pour obtenir un tel effet uniformément sur tout le champ à traiter, il est extrêmement important détablir et de maintenir un contact parfait entre lembout de la sonde et la surface de lexocol. Une fois que la seconde congélation de 3 minutes est achevée, attendez le temps suffisant pour la décongélation avant de retirer la sonde du col. La décongélation est terminée quand il ny a plus de glace sur lembout de la sonde, et celle-ci peut être alors retirée par un délicat mouvement de rotation sur le col. Nessayez surtout pas de retirer la sonde du col avant complète décongélation. Une fois la sonde retirée, vérifiez si le col saigne. La Figure 12.7a montre laspect dun col immédiatement après la cryothérapie. Remarquez la boule de glace qui sest formée dans le col. Après lintervention, il ne faut surtout pas remplir le vagin de gaze ou de coton pour permettre aux sécrétions de sécouler librement. On proposera une serviette hygiénique à la patiente pour éviter que les sécrétions ne tâchent ses vêtements.
Après lemploi, lembout de la sonde doit être essuyée avec de lalcool éthylique ou isopropylique à 60-90%, puis soigneusement nettoyé avec de leau bouillante avant dêtre désinfecté avec du glutaraldehyde à 2% (confère Chapitre 14) et conservé au sec. Une fois lintervention terminée, le pistolet cryogénique, le système de tubes, le manomètre et la bouteille de gaz doivent être décontaminés à laide dun coton imbibé dalcool éthylique ou isopropylique à 60-90%.
 figure 12.5: Positionnement de l'e...
figure 12.5: Positionnement de l'e... figure 12.6: Cryocongélation en co...
figure 12.6: Cryocongélation en co... figure 12.1: Sondes cryogéniques, ...
figure 12.1: Sondes cryogéniques, ... figure 12.2: Equipement de cryothé...
figure 12.2: Equipement de cryothé... figure 12.3: Eléments d'un équipem...
figure 12.3: Eléments d'un équipem... figure 12.4: Unité de cryothérapie...
figure 12.4: Unité de cryothérapie... figure 12.7: (a) Boule de glace su...
figure 12.7: (a) Boule de glace su...Suivi après la cryothérapie
La patiente devra être informée des précautions à prendre et de symptômes éventuels consécutifs au traitement, à savoir des crampes modérées et des pertes liquides claires, parfois légèrement teintées de sang, pendant quatre à cinq semaines après lintervention. Il lui sera également conseillé de ne pas utiliser de douche vaginale ou de tampons, de sabstenir davoir des rapports sexuels pendant le mois qui suit, et de signaler tout symptôme qui apparaîtrait dans les six semaines après le traitement : fièvre pendant plus de deux jours, fortes douleurs pelviennes, pertes vaginales nauséabondes purulentes, caillots de sang, ou saignement pendant plus de deux jours. Il est préférable de donner ces recommandations par écrit.
La cicatrisation a lieu dans les six premières semaines qui suivent la cryothérapie. Pendant les 2-3 premières semaines, on observe lapparition dun tissu granuleux sur la plaie (Figure 12.7b), suivie dune re-épithélialisation de la surface. Normalement, la plaie est totalement cicatrisée au bout de 6 à 8 semaines. Les figures 12.7c et 12.7d montrent laspect du col, respectivement 3 mois et 12 mois après la cryothérapie.
On ne connaît pas leffet de la cryothérapie sur la transmissibilité éventuelle du virus de limmunodéficience humaine (VIH) (à la patiente ou à partir de celle-ci) pendant la phase de cicatrisation. Wright et al., (2001) ont cependant observé la présence de VIH-1 dans les sécrétions vaginales de femmes séropositives traitées par cryothérapie pour une CIN. Ils proposent donc de prévenir toutes les patientes que la cryothérapie peut augmenter la transmissibilité du VIH et que lutilisation du préservatif est un bon moyen de prévention, au moins pendant quatre, voire six, semaines après lintervention. Dans les milieux où linfection à VIH est endémique, lidéal serait de distribuer gratuitement des préservatifs lors des consultations colposcopiques.
La patiente devra prendre rendez-vous pour une visite de contrôle 9 à 12 mois après le traitement, pour vérifier la régression ou la persistance des lésions, grâce à une cytologie et/ou une IVA, suivie dune colposcopie et, selon les résultats de celle-ci, dune biopsie dirigée. Si les lésions persistent, on les traitera à nouveau. Si elles ont disparu, la patiente sera réorientée vers un programme de dépistage (sil existe), ou bien, il lui sera conseillé de faire une visite de contrôle au bout de trois ou cinq ans.
La cicatrisation a lieu dans les six premières semaines qui suivent la cryothérapie. Pendant les 2-3 premières semaines, on observe lapparition dun tissu granuleux sur la plaie (Figure 12.7b), suivie dune re-épithélialisation de la surface. Normalement, la plaie est totalement cicatrisée au bout de 6 à 8 semaines. Les figures 12.7c et 12.7d montrent laspect du col, respectivement 3 mois et 12 mois après la cryothérapie.
On ne connaît pas leffet de la cryothérapie sur la transmissibilité éventuelle du virus de limmunodéficience humaine (VIH) (à la patiente ou à partir de celle-ci) pendant la phase de cicatrisation. Wright et al., (2001) ont cependant observé la présence de VIH-1 dans les sécrétions vaginales de femmes séropositives traitées par cryothérapie pour une CIN. Ils proposent donc de prévenir toutes les patientes que la cryothérapie peut augmenter la transmissibilité du VIH et que lutilisation du préservatif est un bon moyen de prévention, au moins pendant quatre, voire six, semaines après lintervention. Dans les milieux où linfection à VIH est endémique, lidéal serait de distribuer gratuitement des préservatifs lors des consultations colposcopiques.
La patiente devra prendre rendez-vous pour une visite de contrôle 9 à 12 mois après le traitement, pour vérifier la régression ou la persistance des lésions, grâce à une cytologie et/ou une IVA, suivie dune colposcopie et, selon les résultats de celle-ci, dune biopsie dirigée. Si les lésions persistent, on les traitera à nouveau. Si elles ont disparu, la patiente sera réorientée vers un programme de dépistage (sil existe), ou bien, il lui sera conseillé de faire une visite de contrôle au bout de trois ou cinq ans.
 figure 12.7: (a) Boule de glace su...
figure 12.7: (a) Boule de glace su...Prise en charge des femmes pour lesquelles la cryothérapie a échoué
On constate léchec du traitement dans environ 5 à 10% des cas, au cours de la première année de suivi. La persistance de lésions localisées ou multifocales intervient essentiellement si la lésion dorigine était étendue. Pour éliminer léventualité dun carcinome invasif insoupçonné, il est conseillé de faire une biopsie de toutes les lésions persistantes et de traiter à nouveau celles-ci par cryothérapie, RAD, ou conisation à froid, selon les cas. Au cours de la visite de contrôle qui a lieu 9 à 12 mois plus tard, on procèdera à des examens de dépistage (cytologie et/ou IVA) et à une colposcopie. Les patientes ne présentant plus de lésion seront réorientées vers un programme de dépistage (sil y en a un sur la région), ou bien, il leur sera conseillé de refaire une visite de contrôle au bout de trois ou cinq ans. La Figure 11.1 présente un organigramme de prise en charge dans les milieux aux ressources limitées.
 figure 11.1: Flow chart of managem...
figure 11.1: Flow chart of managem...Effets secondaires, complications, et séquelles à long terme
La cryothérapie est généralement indolore si la patiente, préalablement rassurée, coopère et si lintervention est correctement réalisée. Certaines femmes peuvent parfois se plaindre de douleurs pelviennes ou de contractions utérines pendant et après la cryothérapie. De temps en temps, il arrive quune patiente sévanouisse à cause dune réaction vasovagale. Dans ce cas, il ny a pas lieu de saffoler ; la patiente reprendra facilement connaissance.
Dans les 3 à 4 semaines qui suivent lintervention, la patiente se plaindra de pertes vaginales liquides. Les saignements vaginaux sont extrêmement rares. Quand il y en a, ils sont le plus probablement dus à une congélation trop agressive, si bien que la boule de glace a dépassé les 5 mm de profondeur. Le risque dinfection post-opératoire est très faible et peut vraisemblablement être encore réduit en retardant la cryothérapie chez les femmes souffrant dune maladie inflammatoire pelvienne (MIP), dune cervicite sexuellement transmise (par exemple, chlamydia ou gonorrhée), dune trichomoniase vaginale ou dune vaginose bactérienne. On procédera à la cryothérapie une fois ces affections correctement traitées et guéries. Quand une patiente se plaint après lintervention de pertes malodorantes, de douleurs pelviennes et de fièvre, on réalisera une culture à partir des pertes et on prescrira de façon empirique un traitement antibiotique efficace contre les MIP. Les partenaires sexuels devront également être traités si lon diagnostique une cervicite sexuellement transmissible ou une trichomoniase. Dans les pays en développement, par prudence, on peut envisager la prescription dun traitement antibiotique préventif systématique après la cryothérapie (doxycycline 100 mg par voie orale, deux fois par jour, pendant sept jours et métronidazole 400 mg par voie orale, deux fois par jour, pendant sept jours).
La cryothérapie peut être à lorigine dune sténose cervicale chez moins de 1% des patientes et dune diminution de la production de mucus dans 5 à 10% dentre elles. Elle nengendre pas deffet secondaire connu sur la fertilité et la grossesse. Les quelques très rares cas de cancer invasif qui ont pu être détectés après une cryothérapie, étaient généralement la conséquence dune mauvaise évaluation diagnostique avant la cryothérapie.
Dans les 3 à 4 semaines qui suivent lintervention, la patiente se plaindra de pertes vaginales liquides. Les saignements vaginaux sont extrêmement rares. Quand il y en a, ils sont le plus probablement dus à une congélation trop agressive, si bien que la boule de glace a dépassé les 5 mm de profondeur. Le risque dinfection post-opératoire est très faible et peut vraisemblablement être encore réduit en retardant la cryothérapie chez les femmes souffrant dune maladie inflammatoire pelvienne (MIP), dune cervicite sexuellement transmise (par exemple, chlamydia ou gonorrhée), dune trichomoniase vaginale ou dune vaginose bactérienne. On procédera à la cryothérapie une fois ces affections correctement traitées et guéries. Quand une patiente se plaint après lintervention de pertes malodorantes, de douleurs pelviennes et de fièvre, on réalisera une culture à partir des pertes et on prescrira de façon empirique un traitement antibiotique efficace contre les MIP. Les partenaires sexuels devront également être traités si lon diagnostique une cervicite sexuellement transmissible ou une trichomoniase. Dans les pays en développement, par prudence, on peut envisager la prescription dun traitement antibiotique préventif systématique après la cryothérapie (doxycycline 100 mg par voie orale, deux fois par jour, pendant sept jours et métronidazole 400 mg par voie orale, deux fois par jour, pendant sept jours).
La cryothérapie peut être à lorigine dune sténose cervicale chez moins de 1% des patientes et dune diminution de la production de mucus dans 5 à 10% dentre elles. Elle nengendre pas deffet secondaire connu sur la fertilité et la grossesse. Les quelques très rares cas de cancer invasif qui ont pu être détectés après une cryothérapie, étaient généralement la conséquence dune mauvaise évaluation diagnostique avant la cryothérapie.



